Kohlhernie
hernie du chou (franz.); clubroot (engl.)
wissenschaftlicher Name: Plasmodiophora brassicae Wor.
Taxonomie: Chromista, Cercozoa, Phytomyxea, Plasmodiophorida, Plasmodiophoridae
Kohlhernie ist eine typische Fruchtfolgekrankheit, die durch den bodenbürtigen Parasiten Plasmodiophora brassicae verursacht wird. Besonders betroffen sind Flächen auf denen häufig Kreuzblütler (Kruziferen) wie Raps oder Kohlarten angebaut werden. Der Parasit dringt in die Wurzelhaare und später in die Wurzelrinde von Kohlgewächsen ein und verursacht Gewebewucherungen. Die in den Wucherungen gebildeten Dauersporen können im Boden viele Jahre überleben. Ein Kohlhernie Befall kann durch eine weit gestellte Fruchtfolge weitgehend verhindert werden: Auf gefährdeten Böden Raps und andere Kreuzblütler (gilt auch für Zwischenfrüchte) nur alle sieben oder mehr Jahre anbauen. In den Zwischenjahren müssen kreuzblütige Unkräuter, wie Hirtentäschel, Hederich und Ackersenf konsequent bekämpft werden.
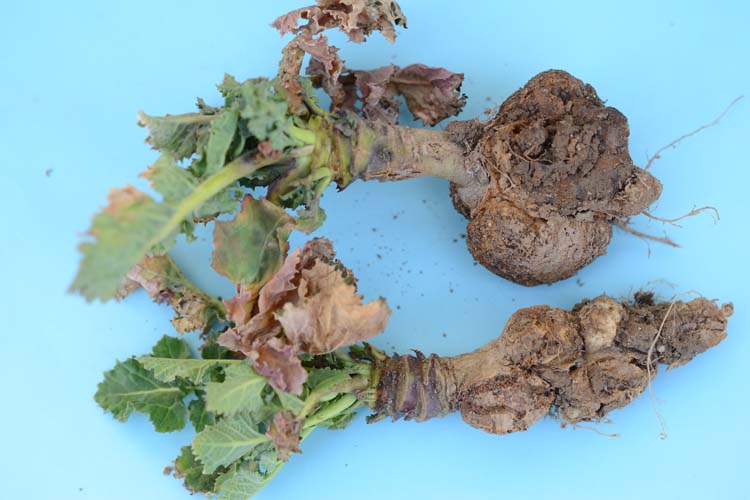
 Abb. 1. Kohlhernie an Raps (Plasmodiophora brassicae)
Abb. 1. Kohlhernie an Raps (Plasmodiophora brassicae)
Krankheitsbild
An Haupt- und Seitenwurzeln der Rapspflanze entstehen keulenförmige Wucherungen (Abb. 1 und 2). Diese äusserlich gefurchten und unregelmässigen Verdickungen sind im Innern weiss, später braun und haben keine Hohlräume. Die Pflanzen entwickeln sich schlecht, haben weniger und kleinere blau-grüne Blätter. Ältere Blätter vergilben. Bei trockener Witterung welken die ansonsten gesund aussehenden Pflanzen. Oft treten die Symptome nesterweise auf, häufig an feuchten Stellen des Ackers.
Verwechslungsmöglichkeit: Der Kohlgallenrüssler (Ceutorhynchus pleurostigma) bildet rundliche, glattwandige Gallen am Wurzelhals und an der Hauptwurzel des Rapses. Im Innern findet man Frassgänge und mit etwas Glück die Larve des Kohlgallenrüsslers.
Krankheitserreger
P. brassicae ist ein obligat biotropher Parasit und kann sich nur in der Wurzel einer Wirtspflanze fortpflanzen. Der Parasit bildet kein Myzel. Die dickwandigen Dauersporen sind bis zu 4 µm gross (Rimmer et al. 2007). Ihre äusserst lange Überlebensdauer verdanken sie einer Sporenwand, die aus Chitin, Proteinen und Lipiden besteht und dadurch einem mikrobiellen Abbau widerstehen kann. Mit dem Auskeimen der Dauerspore werden eine oder mehrere Primär-Zoosporen mit je zwei ungleich langen Peitschengeisseln entlassen. Die Zoosporen sind spindel- bis birnenförmig und 2.8-5.9 µm gross (Kageyama und Asano 2009).
Das Primär-Plasmodium im Wurzelhaar ist vielkernig und wird zum Zoosporangium (Durchmesser 6 – 6.5 µm), das Sekundär-Zoosporen entlässt. Diese infizieren das Rindengewebe, worauf es zur Bildung von unregelmässig geformten (7-90 µm) und runden (5-30 µm) Sekundär-Plasmodien kommt (Abb. 3).
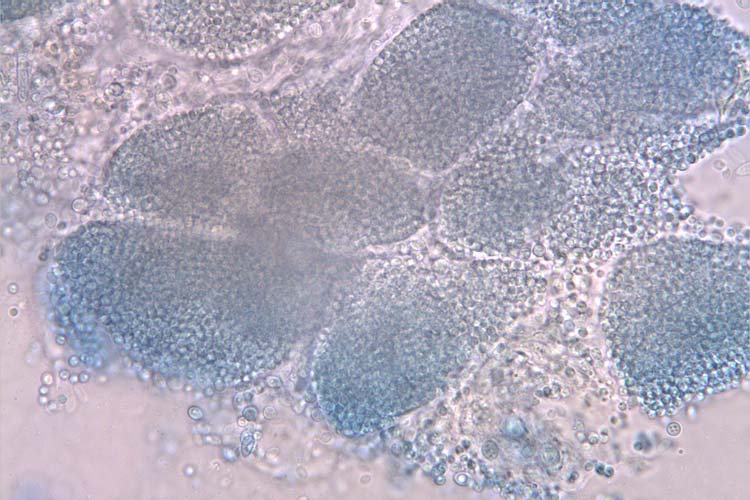 Abb. 3. In den Verdickungen an Haupt- und Seitenwurzeln befinden sich Plasmodien, die Dauersporen entlassen.
Abb. 3. In den Verdickungen an Haupt- und Seitenwurzeln befinden sich Plasmodien, die Dauersporen entlassen.
Lebenszyklus
Plasmodiophora brassicae ist ein bodenbürtiger, obligater Parasit. Der Krankheitserreger durchläuft während eines Lebenszyklus drei Stadien: Überleben im Boden als Dauerspore, Wurzelhaarinfektion und Infektion der Wurzelrinde (Kageyama und Asano 2009).
Die haploiden Dauersporen können sehr lange im Boden überleben. In der Gegenwart von geeigneten Wirtspflanzen keimen diese im Boden und entlassen je eine oder mehrere Primär-Zoosporen. Diese bewegen sich aktiv im Bodenwasser. Treffen sie auf ein Wurzelhaar einer Wirtspflanze, dringen sie durch die Zellwand in das Innere der Wurzelhaarzelle ein, wobei sie die Geisseln vorgängig abstossen. Dort wächst jede einzelne dieser amöbenartigen Zellen zu einem vielkernigen Primär-Plasmodium heran. Dieses kann sich teilen und von Pflanzenzelle zu Pflanzenzelle weiterwandern. Später zergliedern sich die Plasmodien in Zoosporangien, die je 4-16 begeisselte Sekundär-Zoosporen in den Boden entlassen. Diese Sekundär-Zoosporen lösen neue Infektionen aus. Sie durchdringen die Wurzelepidermis und besiedeln das Rindengewebe der Hauptwurzel.
P. brassicae scheidet Auxine, Cytokinine und andere pflanzliche Wachstumshormone aus, welche eine abnormale Vermehrung und Vergrösserung der Pflanzenzellen in den Wurzeln auslösen und damit die charakteristischen Wucherungen verursachen. Innerhalb der Rindenzellen werden Sekundär-Plasmodien gebildet. Diese Plasmodien zerfallen schliesslich innerhalb der Wurzelgallen in Millionen von Dauersporen. Mit dem Zerfall des Wurzelgewebes werden diese in den Boden entlassen. Dauersporen können bis zu 20 Jahre im Boden überleben (Hwang et al. 2012).
Epidemiologie
Eine hohe Bodenfeuchtigkeit und eine Bodentemperatur von über 20 °C fördern den Befall mit Kohlhernie. Insbesondere ist für die Fortbewegung der Zoosporen freies Wasser erforderlich.
Eine saure Bodenreaktion fördert die Keimung der Dauersporen und die Entwicklung der Plasmodien.
Wirtsspektrum
Plasmodiophora brassicae befällt alle Kreuzblütler (Brassicaceae) (Hwang et al. 2012). Neben Raps sind dies zum Beispiel alle Kohlarten (Brassica oleracea). Auch Unkräuter aus der Familie der Kreuzblütler wie das Hirtentäschchen (Capsella bursa-pastoris), das Acker-Täschelkraut (Thlaspi arvense), Hederich (Raphanus raphanistrum), Ackersenf (Sinapis arvensis) sind Wirtspflanzen.
Vorbeugende Massnahmen
- Eine weit gestellte Fruchtfolge mit einem drei bis vierjährigen Unterbruch zwischen Brassica Kulturen ist wichtig, um die Wahrscheinlichkeit eines Kohlhernie Befalls zu reduzieren. Das Auftreten von Kohlhernie sollte unbedingt vermerkt werden, um die weitere Verbreitung über kontaminierte Erde zu verhindern. Flächen mit Befall sollten zuletzt bearbeitet werden und die verwendeten Maschinen müssen gereinigt werden.
- Keine Kreuzblütler als Zwischenkulturen anbauen.
- Konsequente Bekämpfung von Unkräutern aus der Familie der Kreuzblütler während der ganzen Fruchtfolge. Auch Ausfallraps trägt zur Vermehrung des Erregers im Boden bei und sollte bis zum 4-Blatt-Stadium beseitigt werden.
- Bodenverdichtungen und damit Staunässe vermeiden
- Eine Kalkung mit Calciumcarbonat hebt die Bodenreaktion. Ein pH-Wert des Bodens von 7.2 reduziert in der Regel die Entwicklung des Parasiten und den Befall durch die Kohlhernie (Donald und Porter 2009).
- Die Anwendung von Kalkstickstoff (Calciumcyanamid) hat eine abtötende Wirkung auf die Kohlhernie. Kalkstickstoff hat nur eine begrenzte Wirkung, der Krankheitsdruck wird allerdings verringert (Donald und Porter 2009).
- Gründüngung, die untergepflügt wird, kann die Kohlhernie reduzieren
- Im Gemüsebau sollte die Erde für die Anzucht der Setzlinge sterilisiert werden.
- Resistente Sorten anbauen. In der Liste der für die Schweiz empfohlenen Rapssorten (für Deutschland Sortenlisten des Bundessortenamtes) sind auch Sorten aufgeführt, die exklusiv für den Anbau auf mit Kohlhernie infizierten Parzellen zugelassen sind.
- Früh gesäter Raps wird häufiger und stärker befallen als spät gesäter. Kühle Temperaturen hemmen Keimung und Wachstum des Erregers.
Literatur
Donald C, Porter I, 2009. Integrated Control of Clubroot. Journal of Plant Growth Regulation 28: 289-303.
Hwang SF, Strelkov SE, Feng J, Gossen BD, Howard RJ, 2012. Plasmodiophora brassicae: a review of an emerging pathogen of the Canadian canola (Brassica napus) crop. Molecular Plant Pathology 13 (2): 105-113.
Kageyama K, Asano T, 2009. Life cycle of Plasmodiophora brassicae. Journal of Plant Growth Regulation 28: 203–211.
Rimmer SR, Shattuck VI, Buchwaldt L, 2007. Compendium of Brassica Diseases. The American Phytopathological Society Press, St. Paul: 117S.




