Echter Mehltau der Kürbisgewächse
oïdium des cucurbitacées (franz.); powdery mildew (engl.)
wissenschaftliche Namen:
Podosphaera xanthii (Castagne) U. Braun & Shishkoff (Synonyme Sphaerotheca fusca und S. fuliginea)
Golovinomyces cichoracearum (DC.) V.P. Heluta var cichoracearum (Synonym Erysiphe cichoracearum)
Leveillula taurica (anamorph = Oidiopsis taurica)
Taxonomie: Fungi, Ascomycota, Leotiomycetes, Erysiphales, Erysiphaceae
Kürbisgewächse werden hauptsächlich von zwei Arten der Echten Mehltaupilzen befallen: Golovinomyces cichoracearum und Podosphaera xanthii. Gelegentlich kommt auch eine dritte Art, Leveillula taurica, vor. Diese ist jedoch von geringer wirtschaftlicher Bedeutung. Der Echte Mehltau befällt vorwiegend die Blätter, wo er die gesamte Blattoberseite mit einem weissen, mehligen Pilzgeflecht bedecken kann. In den letzten Jahren haben die Pflanzenzüchter die Resistenz von Kürbisgewächsen gegen den Echten Mehltau jedoch so stark verbessert, dass es für alle Arten leistungsstarke, resistente Sorten gibt.
 Abb. 1. Echter Mehltau an Zucchetti
Abb. 1. Echter Mehltau an Zucchetti
 Abb. 2. Echter Mehltau an Gurke
Abb. 2. Echter Mehltau an Gurke
Schadbild und Schadwirkung
Die ersten Anzeichen eines Befalls mit Echtem Mehltau sind rundliche, weisse, pulverförmige Flecken auf der Blattoberseite (Abb. 3, 4 und 5). Diese vergrössern sich rasch und bedecken schliesslich das gesamte Blatt mit einem mehligen Pilzgeflecht (Bedlan und Kahrer 2002) (Abb. 1 bis 5). Ein Befall der Blattstiele und Früchte ist ebenfalls möglich (Schwarz et al. 1990). Im Gewächshaus, zum Teil auch im Freiland, kann der Pilzbelag ebenfalls auf der Blattunterseite vorkommen, dies im Gegensatz zu den meisten anderen Echten Mehltaupilzen. Mit zunehmendem Alter wird der Belag grau und später braun. Befallene Blätter vergilben und sterben ab.
Gelegentlich können im Spätsommer auf alten Mehltaubelägen Kleistothecien (sexuell entstandene Fuchtkörper des Pilzes) beobachtet werden.
Die beiden Echten Mehltaupilze (P. xanthii und G. cichoracearum) können zusammen vorkommen. Im Freiland kommt meist G. cichoracearum, im Gewächshaus eher P. xanthii vor (Bedlan und Kahrer 2002).
Schadwirkung: Echter Mehltau ist weit verbreitet. In der Regel tritt er erst spät auf, so dass keine grossen Ertragseinbussen zu erwarten sind (Schwarz et al. 1990).
Beschreibung der Krankheitserreger
Kürbisgewächse werden hauptsächlich von zwei verschiedenen Arten der Echten Mehltaupilzen befallen: Golovinomyces cichoracearum und Podosphaera xanthii. Beide Arten bilden ein weissliches Myzel auf der Blattoberfläche, wo auch die Konidienträger entstehen (Abb. 6).
Bei G. cichoracearum werden Konidien in langen Ketten gebildet (Abb. 7), die farblos (hyalin) sind, eine ellipsoide bis tonnenförmige Form haben und eine Grösse von 25–45 x 14–25 µm aufweisen (Koike et al. 2007). Die Randlinien der unreifen Konidienketten sind gewellt und die Konidien weisen keine Fibrosinkörper auf. Die Konidien von G. cichoracearum keimen mit geraden Keimschläuchen und bilden ungelappte Appressorien aus. Kleistothecien werden selten beobachtet. Sie sind kugelförmig, haben zahlreiche hyphenartige Fortsätze und enthalten bis zu 10–25 einwandige Asci. Diese enthalten zwei eiförmige bis ellipsoide Ascosporen.
Auch die Konidien von P. xanthii werden in langen Ketten gebildet. Sie sind farblos (hyalin), ellipsoid bis tonnenförmig und messen 25–37 x 14–25 µm (Koike et al. 2007). Ihre Randlinien sind gezackt und frisch gebildete Konidien enthalten Fibrosinkörper. Diese lassen sich am besten in frischen Konidien beobachten, die in einer 3-prozentigen KOH-Lösung fixiert sind (Keinath et al. 2017). Konidien von P. xanthii bilden bei der Keimung gegabelte Keimschläuche, jedoch keine Appressorien. Kleistothecien sind selten. Sie sind ebenfalls kugelförmig, haben zahlreiche verzweigte Fortsätze (Keinath et al. 2017) und enthalten einen einzigen einwandigen Ascus mit acht eiförmigen Ascosporen. P. xanthii scheint weltweit häufiger vorzukommen.
Grundsätzlich haben G. cichoracearum und P. xanthii ein breites Wirtsspektrum. Beide Arten sind jedoch sehr komplex. Einzelne Populationen innerhalb jeder Art sind vermutlich wirtsspezifisch und befallen nur bestimmte Pflanzengruppen. Isolate von G. cichoracearum und P. xanthii, die von Kürbisgewächsen stammen, können höchstwahrscheinlich keine Nicht-Kürbisgewächse befallen und umgekehrt (Koike et al. 2007).
Einige Kürbisgewächse (wie Gurken) sind auch anfällig für eine dritte Art von Echtem Mehltau: Leveillula taurica (Anamorph: Oidiopsis taurica). Dieser Pilz ist jedoch von geringer wirtschaftlicher Bedeutung. Er verursacht chlorotische, von Adern begrenzte Blattflecken. Auf der Unterseite dieser eckigen Flecken entwickelt sich eine reichliche weisse Sporenbildung.
 Abb. 6. Konidienträger und Konidien des Echten Mehltaus von Kürbisgewächsen
Abb. 6. Konidienträger und Konidien des Echten Mehltaus von Kürbisgewächsen
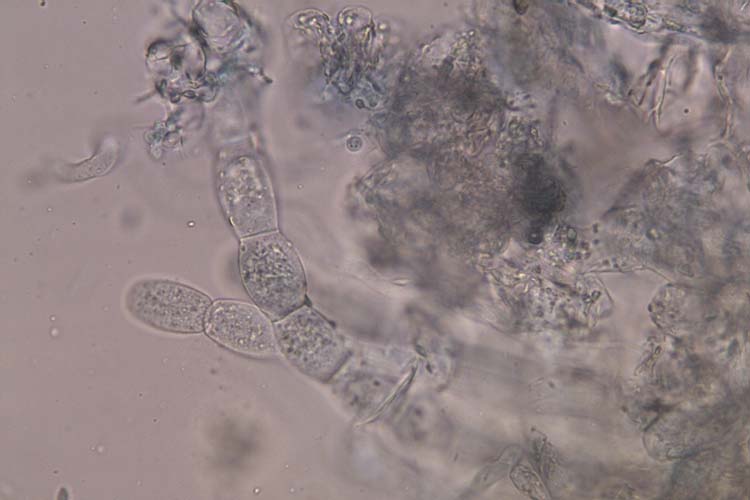 Abb. 7. Konidienträger mit Konidien des Echten Mehltaus von Kürbisgewächsen
Abb. 7. Konidienträger mit Konidien des Echten Mehltaus von Kürbisgewächsen
Lebenszyklus
Echte Mehltaupilze sind obligate Parasiten, das heisst, sie können sich nur von lebenden Wirtspflanzen ernähren. Als primäre Infektionsquelle im Frühjahr gelten Konidien, die sich ausgehend von infizierten Kürbisgewächsen über grosse Entfernungen ausbreiten (Koike et al. 2007). Weitere mögliche Quellen sind in Gewächshäusern angebaute Kürbisgewächse. Konidien bleiben 7–8 Tage lang lebensfähig und werden vom Wind über weite Strecken verbreitet. Die Bedeutung der Kleistothecien als Infektionsquelle ist wahrscheinlich vernachlässigbar, da sie eher selten gebildet werden und die Ernterückstände nach der Ernte in den Boden eingearbeitet werden.
Wenn die Konidien auf eine Wirtspflanze gelangen, keimen sie aus und bilden auf den Blättern Haftorgane (Appressorien) aus (P. xanthii bildet keine). Unmittelbar darunter dringt eine Infektionshyphe durch die Kutikula und die Zellwand der Epidermiszelle. In den Epidermiszellen bildet der Pilz Haustorien, die ihm zur Nahrungsaufnahme dienen. Das Myzel der Echten Mehltaupilze wächst an der Pflanzenoberfläche und bildet reichlich Konidien, die wiederum gesunde Wirtspflanzen befallen können.
Unter trockenen und warmen Bedingungen können die Echten Mehltaupilze sehr schnell wachsen. Eine längere Blattnässedauer hemmt hingegen ihre Entwicklung. In der Regel beträgt die Zeit zwischen der Infektion und dem Auftreten der Symptome nur 3-7 Tage (Keinath et al. 2017).
Wirtsspektrum
G. cichoracearum und P. xanthii befallen verschiedene Kürbisgewächse: darunter Gurke (Cucumis sativus), Melone (Cucumis melo), Wassermelone (Citrullus lanatus) sowie Kürbis / Zucchini (Cucurbita spp.) (Crüger et al. 2002). Siehe auch Kapitel «Beschreibung des Krankheitserregers».
Vorbeugende Massnahmen und Bekämpfung
- Resistente oder tolerante Sorten pflanzen (Herren et al. 2025)
- Trockene Bedingungen fördern die Ausbreitung der Echten Mehltaupilze. Trotzdem sollte morgens und abends die Luftfeuchtigkeit gesenkt werden, um einen Befall durch den Falschen Mehltau zu vermeiden.
- Befallene Pflanzenrückstände beseitigen oder gut kompostieren.
- Pflanzenschutzmittel nur bei frühem und starkem Befall einsetzen. Wartezeiten beachten!
- Der Einsatz von Kaliumhydrogencarbonat, Schwefel, Fenchelöl oder FytoSave (die beiden letzteren nur im Gewächshaus) ist im Biogemüsebau in der Schweiz möglich (Betriebsmittelliste für den biologischen Anbau in der Schweiz und Deutschland). Achtung: Schwefel kann in hohen Konzentrationen Nützlinge schädigen.
- Zugelassene Pflanzenschutzmittel zum Schutz der Kürbisgewächse gegen den Echten Mehltau (Golovinomyces cichoracearum und Podosphaera xantii) finden Sie für die Schweiz im Pflanzenschutzmittelverzeichnis des BLV; für Deutschland in der online-Datenbank Pflanzenschutzmittel des BVL und für Österreich im Pflanzenschutzmittelregister des BAES.
Literatur
Bedlan G, Kahrer A, 2002. Wichtige Krankheiten und Schädlinge im Gemüsebau. Verlag Jugend & Volk GmbH, Wien: 248 S.
Crüger G, Backhaus GF, Hommes M, Smolka S, 2002. Pflanzenschutz im Gemüsebau. 4.
Herren, P. et al. (2025). Pflanzenschutzempfehlungen für den Biogemüsebau. Forschungsinstitut für biologischen Landbau FiBL, Frick. shop.fibl.org (aktuelle Ausgabe)
Keinath AP, Wintermantel WW, Zitter TA, 2017. Compendium of Cucurbit Diseases and Pests. Second edition. The American Phytopathological Society, St. Paul Minnesota: 127 p.
Koike ST, Gladders P, Paulus AO, 2007. Vegetable Diseases. A colour Handbook. Manson Publishing Ltd., 448 p.
Schwarz A, Etter J, Künzler R, Potter C, Rauchstein HR, 1990. Pflanzenschutz im integrierten Gemüsebau. Verlag Landwirtschaftliche Lehrmittelzentrale, 3052 Zollikofen, 321 S.



