Schwarzfäule
Pourriture des feuilles de la base (franz.); bottom rot (engl.)
wissenschaftliche Namen: Rhizoctonia solani Kühn (asexuelle Form);
Thanatephorus cucumeris (A.B. Frank) Donk (sexuelle Form)
Taxonomie: Fungi, Basidiomycota, Agaricomycetes, Cantharellales, Ceratobasidiaceae
Der Verursacher der Schwarzfäule ist der Pilz Rhizoctonia solani. Der Krankheitserreger ist ein Bodenbewohner, der als Myzel oder als Sklerotium in und auf Ernterückständen im Boden überlebt. Die Krankheit entwickelt sich, wenn die Salatblätter mit dem befallenen Boden in Kontakt kommen. Zunächst beginnen die unteren Blätter zu faulen. Später breitet sich der Pilz rasch aus und dringt in das Innere der Köpfe ein, was zur Fäulnis der gesamten Pflanze führt. Der Strunk ist der letzte Teil des Kopfes, der verfault. Um einen Befall mit Schwarzfäule möglichst zu verhindern, sind eine ausreichende Fruchtfolge, der Anbau von Salat auf Hochbeeten oder der Einsatz von Mulchfolien sowie die Einarbeitung der Ernterückstände wichtige Massnahmen.
 Abb. 1. Schwarzfäule (Rhizoctonia solani) an Eisbergsalat: Fäulnis an den Blättern, die auf dem Boden aufliegen
Abb. 1. Schwarzfäule (Rhizoctonia solani) an Eisbergsalat: Fäulnis an den Blättern, die auf dem Boden aufliegen
 Abb. 2. Schwarzfäule (R. solani) an Eisbergsalat
Abb. 2. Schwarzfäule (R. solani) an Eisbergsalat
Schadbild
Rhizoctonia solani befällt alle Salattypen, einschliesslich Endivie (Subbarao et al. 2017).
Der Krankheitserreger kann bei Jungpflanzen die sogenannte Umfallkrankheit auslösen. Dabei beginnen die Wurzeln zu faulen, sodass die Pflanzen nesterweise umfallen.
Am häufigsten tritt die Schwarzfäule jedoch bei reifen oder kurz vor der Reife stehenden Pflanzen auf. Typischerweise treten die Krankheitssymptome zuerst an den unteren Blättern auf, die in direktem Kontakt mit dem Boden stehen (Abb. 1 und 2). Zu den Symptomen einer Infektion gehören kleine, rostfarbene bis schokoladenbraune Flecken, die sich vorwiegend auf der Unterseite der Blattmittelrippen befinden (Subbarao et al. 2017). Später verfaulen die äusseren Blätter, werden dünn und verfärben sich braunschwarz (Crüger et al. 2002). Die Mittelrippen der Blätter bleiben relativ lange erhalten und weisen bräunliche Längsstreifen auf. Unter günstigen Temperatur- und Feuchtigkeitsbedingungen kann sich die Schwarzfäule rasch ausbreiten und die inneren Blätter des Kopfes befallen. Dies führt zu einer Fäulnis der gesamten Pflanze. Verfaulende Köpfe werden fast schwarz, wenn sie zusammenfallen und austrocknen. Der Strunk ist etwas widerstandsfähiger gegen die Besiedlung durch den Erreger und verfault deshalb als letzter Teil des Kopfes.
Die durch die Infektion verursachten Schäden bieten zudem Eintrittsstellen für sekundäre Fäulniserreger, insbesondere für Weichfäulebakterien. Diese Organismen können für den raschen Verfall verantwortlich sein, der in späteren Stadien der Schwarzfäule beobachtet wird.
Verwechslungsmöglichkeit: Die Schwarzfäule wird oft mit der Graufäule (Botrytis cinerea) und der Sclerotinia-Fäule (Sclerotinia spp.) verwechselt.
Beschreibung des Krankheitserregers
Die Schwarzfäule wird durch den Bodenpilz Rhizoctonia solani (Hauptfruchtform: Thanatephorus cucumeris) verursacht (Subbarao et al. 2017). Die Hyphen von R. solani sind weiss bis braun und septiert und verzweigen sich typischerweise fast rechtwinklig (Abb. 3). Unmittelbar nach der Verzweigung bildet sich eine Querwand. Die Verzweigungen sind auffällig eingeschnürt. R. solani bildet weder asexuelle Fruchtkörper noch Sporen. Die Hyphen vernetzen sich zum Myzel. In diesem bilden sich hellbraune bis dunkelbraune Sklerotien (Dauerkörper).
Das sexuelle Stadium (T. cucumeris) wird auf Salat nur selten gebildet (Koike et al. 2007). Dabei bildet sich auf der Pflanzenoberfläche eine weisse Fruchtschicht, die aus Basidien (8–11 x 18–23 µm) besteht. Diese schnüren farblose, einzellige Basidiosporen (4–7 × 7–13 µm) ab.
Isolate von R. solani werden in 13 unterschiedliche Gruppen, die als Anastomosegruppen (AG) bezeichnet werden, unterteilt (Tsor 2010). Innerhalb einer AG können die Hyphen erfolgreich miteinander verschmelzen (=Anastomosen), zwischen Isolaten verschiedener Gruppen ist dies jedoch nicht möglich. Je nach Zugehörigkeit zu einer bestimmten AG kann R. solani unterschiedliche Kulturen befallen oder unterschiedliche Symptomausprägungen (Virulenz) verursachen.
AG 1-1B wurde in Deutschland am häufigsten aus infiziertem Salat isoliert, zusammen mit AG 1-1C und AG 2-1 (Grosch et al. 2004). Isolate der AG 1-1B verursachten zudem eine starke Symptomausprägung bei Spinat, Brokkoli, Radieschen, Kohlrabi und Hirse, jedoch nur eine geringe Symptomausprägung bei Mais, Tomaten und Zwiebeln. Kenntnisse über das Wirtsspektrum der vorhandenen AG sind wichtig für die Planung einer wirksamen Fruchtfolge als Teil der Bekämpfungsstrategie.
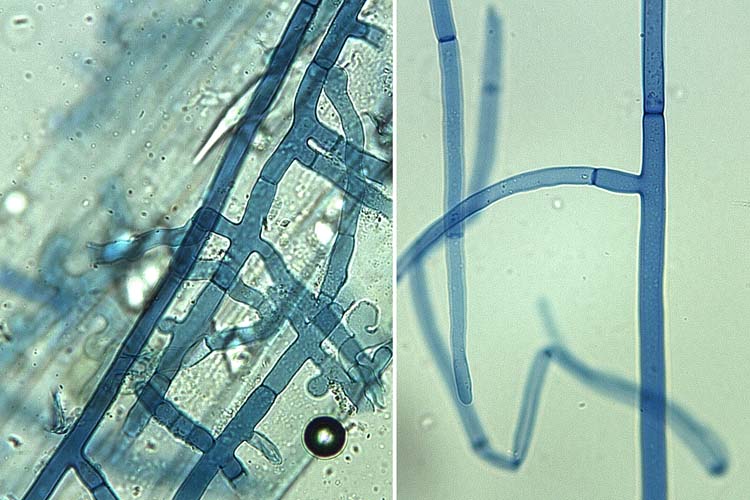 Abb. 3. Rhizoctonia solani bildet ein stark verzweigtes Myzel. Die Verzweigungen der Haupthyphen stehen rechtwinklig zueinander.
Abb. 3. Rhizoctonia solani bildet ein stark verzweigtes Myzel. Die Verzweigungen der Haupthyphen stehen rechtwinklig zueinander.
Lebenszyklus
Der Erreger der Schwarzfäule ist ein Bodenbewohner, der als Myzel oder Sklerotien in und auf Ernterückständen im Boden überlebt. Er kann mit infiziertem Boden über grosse Entfernungen verbreitet werden, insbesondere in Form von Sklerotien. Auch Basidiosporen sind zur Ausbreitung über große Entfernungen fähig (Subbarao et al. 2017).
Unter günstigen Feuchtigkeits- und Temperaturbedingungen keimen die Sklerotien und bilden Myzel aus, das bis zu 10 cm wachsen kann, um eine Nahrungsquelle zu erreichen. R. solani kann direkt über gesundes oder verletztes Gewebe oder durch Spaltöffnungen in die Pflanze eindringen. Die Krankheit entwickelt sich, wenn die unteren Salatblätter mit befallenem Boden in Kontakt kommen.
Epidemiologie
Warme, feuchte Bedingungen begünstigen die Entwicklung der Schwarzfäule. Das optimale Myzelwachstum findet bei Temperaturen zwischen 20 und 30 °C (Optimum 25 °C) sowie über einen breiten pH-Bereich von pH 5 bis pH 8 statt (Subbarao et al. 2017). Der Zeitraum von der Infektion bis zur ersten Symptomausprägung kann 36 bis 48 Stunden oder länger betragen.
Das Auftreten der Schwarzfäule wird stark von der Vorfrucht, der Zeit zwischen den anfälligen Kulturen, der Virulenz der vorhandenen Isolate (siehe Kapitel Beschreibung des Krankheitserregers) sowie deren Überlebensfähigkeit im Boden beeinflusst.
Wirtsspektrum
Rhizoctonia solani ist eine Sammelart mit einem sehr grosse Wirtspflanzenkreis. Zu den Wirtspflanzen gehören neben Salat, inklusive Endivie, auch Kartoffeln (Wurzeltöterkrankheit), Zuckerrüben (Auflaufkrankheiten, Späte Rübenfäule), Weizen, Reis, Mais, Sorghum und Soja. Je nach Anastomosegruppe befällt R. solani unterschiedliche Wirtspflanzen. Nach Grosch et al. (2004) war AG 1-1B in Deutschland die häufigste Anastomosegruppe an Salat. Sie befällt unter anderem auch Reis, Bohnen, Sojabohnen und Kohlgewächse.
Vorbeugende Massnahmen und Bekämpfung
- Eine Fruchtfolge mit Nichtwirtspflanzen verringert das Inokulum im Boden.
- Der Anbau von Salatsorten mit aufrechter Wuchsform verringert das Risiko eines starken Befalls durch die Schwarzfäule.
- Der Anbau von Salat auf Hochbeeten oder der Einsatz von Mulchfolien verbessert die Belüftung und minimiert den Kontakt der Blätter mit dem Boden.
- Pflanzen Sie in gut durchlässigen Boden und vermeiden Sie übermässige Bewässerung. Eine gute Entwässerung und Unkrautbekämpfung sind ebenfalls wichtig.
- Durch das Einarbeiten der Ernterückstände werden die Sklerotien vergraben und ihre Lebensfähigkeit nimmt ab.
- Zugelassene Pflanzenschutzmittel zum Schutz von Salat gegen die Schwarzfäule (Rhizoctonia solani) finden Sie für die Schweiz in der Betriebsmittelliste für den biologischen Anbau sowie im Pflanzenschutzmittelverzeichnis des BLV. Für Deutschland finden Sie diese in der Online-Datenbank des BVL und für Österreich im Pflanzenschutzmittelregister des BAES.
Literatur
Crüger G, Backhaus GF, Hommes M, Smolka S, 2002. Pflanzenschutz im Gemüsebau. 4. Auflage, Verlag Eugen Ulmer Stuttgart: 318 S.
Grosch R, Schneider JHM, Kofoet A, 2004. Characterization of Rhizoctonia solani anastomosis groups causing bottom rot in field-grown lettuce in Germany. Eur. J. Plant Path. 110: 53-62.
Koike ST, Gladders P, Paulus AO, 2007. Vegetable Diseases. A colour Handbook. Manson Publishing Ltd., 448 p.
Subbarao KV, Davis RM, Gilbertson RL, Raid RN, 2017. Compendium of lettuce diseases and pests. The disease compendium series of the American Phytopathological Society, second edition, APS Press St. Paul Minnesota: 165 p.
Tsror L, 2010. Biology, Epidemiology and Management of Rhizoctonia solani on Potato. Journal of Phytopathology 158: 649-658.



